脑室是脑的“窗口”,脑室的形态变化反映了脑的发育及老化过程,异常的脑室形态与多种神经及精神系统疾病息息相关。最新的研究表明认知障碍、注意缺陷多动障碍、孤独症谱系障碍、双相情感障碍、重度抑郁障碍和精神分裂症患者中均可见脑室形态异常。
因此,探索脑室形态的遗传结构可加深对脑疾病内在机制的理解,进而协助医生及患者早期诊断及治疗脑疾病,促进脑健康。
10月19日,实验室程炜研究员团队联合复旦大学附属华山医院郁金泰教授团队,与国际多中心多学科交叉融合团队协作,基于覆盖全生命周期的五大队列六万余名参与者的遗传和神经影像数据,揭示了脑室形态的遗传基础,发现了脑室形态与神经精神疾病存在遗传关联。并且该研究首次提出侧脑室下角体积增大是阿尔茨海默病可遗传的内表型,可独立于海马体积等传统影像标志物早期预测阿尔茨海默病的发病风险,具有临床应用价值。
相关研究成果以《脑室的遗传结构及其与神经精神特征的遗传重叠》(“Genetic architectures of cerebral ventricles and their overlap with neuropsychiatric traits”)为题发表在Nature子刊《Nature Human Behaviour》。

研究团队首先利用31,880位参与者的遗传和颅脑核磁共振数据,对侧脑室体积、侧脑室下角体积、第三脑室体积、第四脑室体积、侧脑室不对称性、侧脑室下角不对称性进行分析,发现了62个影响脑室形态的遗传位点和785个候选基因,并在包括23,533人的独立队列中验证了超过80%的影响侧脑室体积的位点。进一步分析提示脑室的体积及不对称性均可遗传(遗传力3%-40%),与脑室相关的基因同时在脑的发育和衰老通路中富集。

▲ 与脑室形态相关的位点的特征
“脑室扩大并不等同于脑萎缩。由于大脑皮质神经元起源于胚胎脑室的干细胞,因此脑室形态异常也有可能是神经系统发育异常的后果。因此,有必要对覆盖全生命周期的样本进行分析,以了解影响脑室形态的基因组位点在全生命周期中的作用,这正是既往研究所欠缺的部分。” 该研究项目的共同通讯作者,复旦大学附属华山医院郁金泰教授表示。
进一步,研究团队在分析中加入儿童、青少年、青年队列及纵向数据,探究遗传因素在全生命周期对脑室的影响。研究结果显示,chr3q28位点主要参与脑室发育,而chr7p22.3和chr16q24.2位点可能在脑室的老化过程发挥作用。
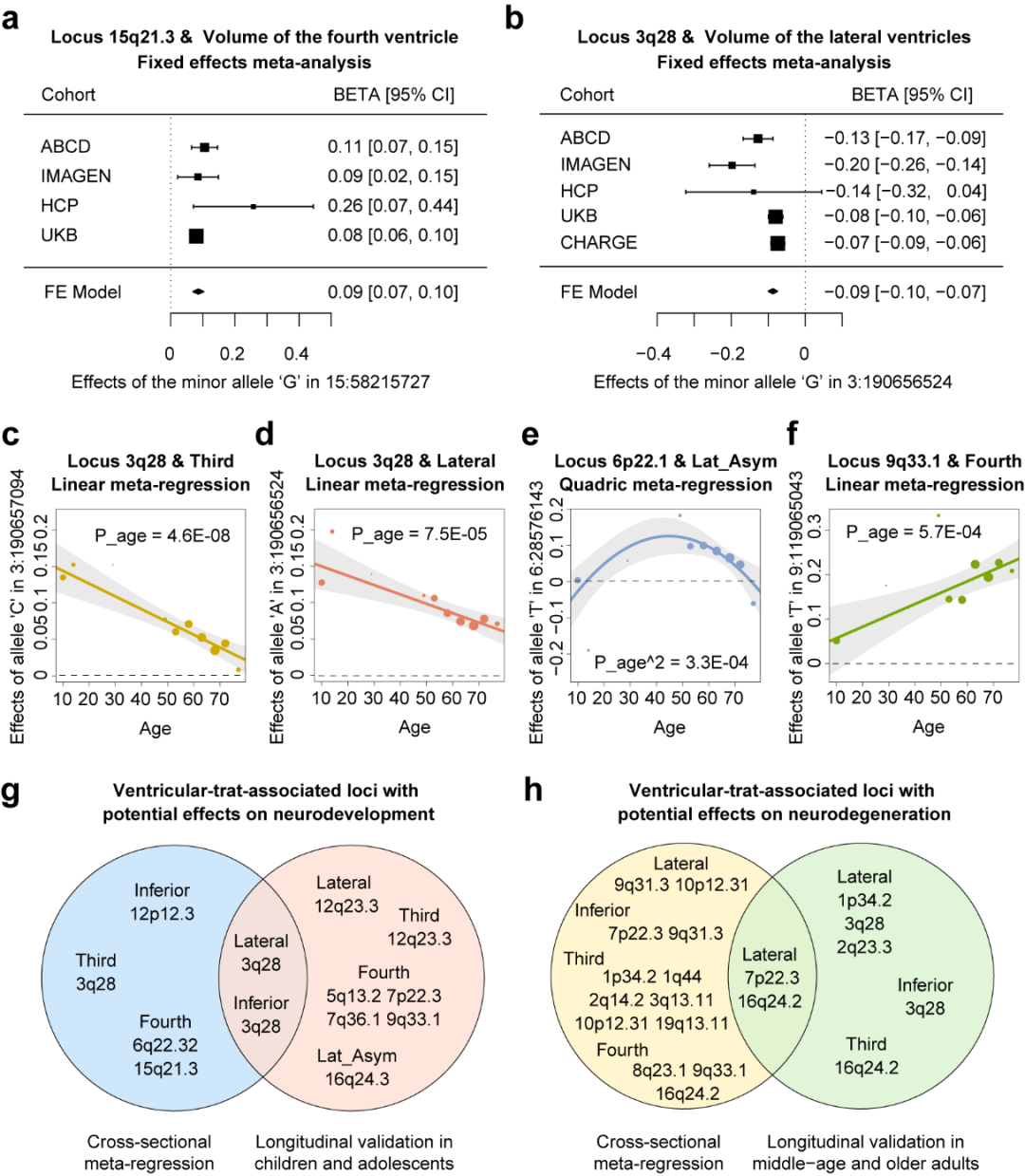
▲全生命周期分析发现了3个主要影响脑室发育或老化的位点
共同通讯作者程炜研究员解释:“通过整合全生命周期的数据,我们研究发现部分位点在全生命周期中对脑室形态产生不同的影响,该结果将有助于理解年龄相关疾病的神经机制。例如,主要影响老年人脑室形态改变的位点更有可能与脑的衰老和认知下降等病理过程有关。”
为了探索脑室形态和神经精神特征之间的遗传重叠,进而理解脑室形态影响脑疾病发生的遗传机制,研究团队进而联合多种统计方法检验脑室形态特征与神经精神特征的关联。连锁不平衡分数回归(LDSC)提示脑室体积与反应时间、皮质厚度等特征存在遗传相关性。
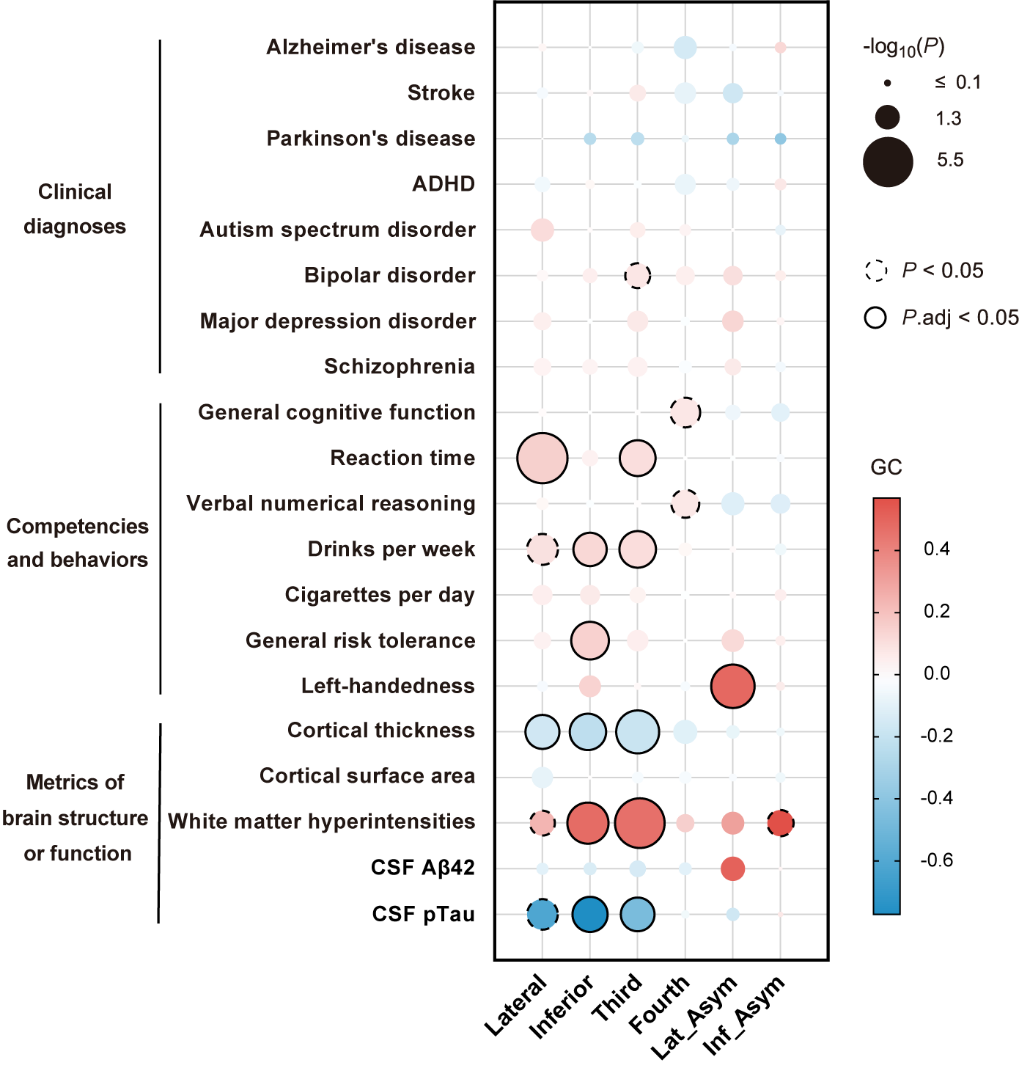
▲脑室形态与多种认知行为特征及反映脑功能的指标存在遗传相关性
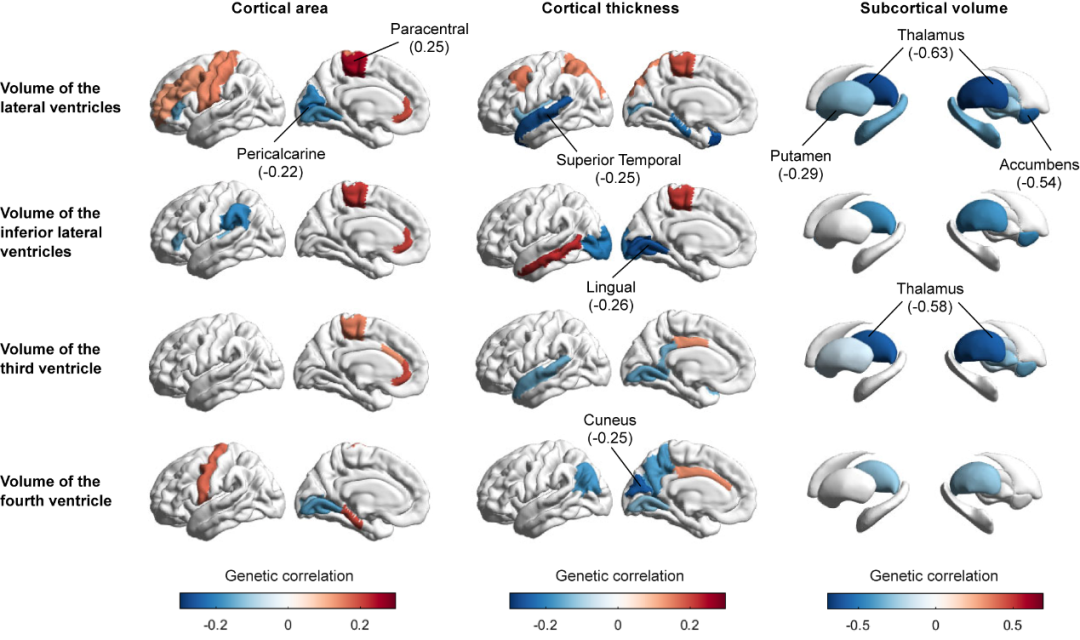
▲脑室形态与皮层表面积、皮层厚度、皮层下体积存在遗传相关性
进一步,多基因风险评分(PRS)分析提示阿尔茨海默病高遗传风险的个体更有可能表现出较大的侧脑室下角体积。双向孟德尔随机化(MR)提示较大的侧脑室下角体积可能是高阿尔茨海默病遗传风险导致的后果。生存分析(COX)从临床角度证实了较大的侧脑室下角体积可预测阿尔茨海默病的发病风险。最后,为了验证结果的可靠程度,研究团队通过事后分析进一步检验了侧脑室下角体积与阿尔茨海默病的关联。结果提示侧脑室下角体积对阿尔茨海默病发病风险的预测价值独立于海马体积,且该关联能在独立队列中得到验证。同时,侧脑室下角体积与阿尔茨海默病的家族史有关。
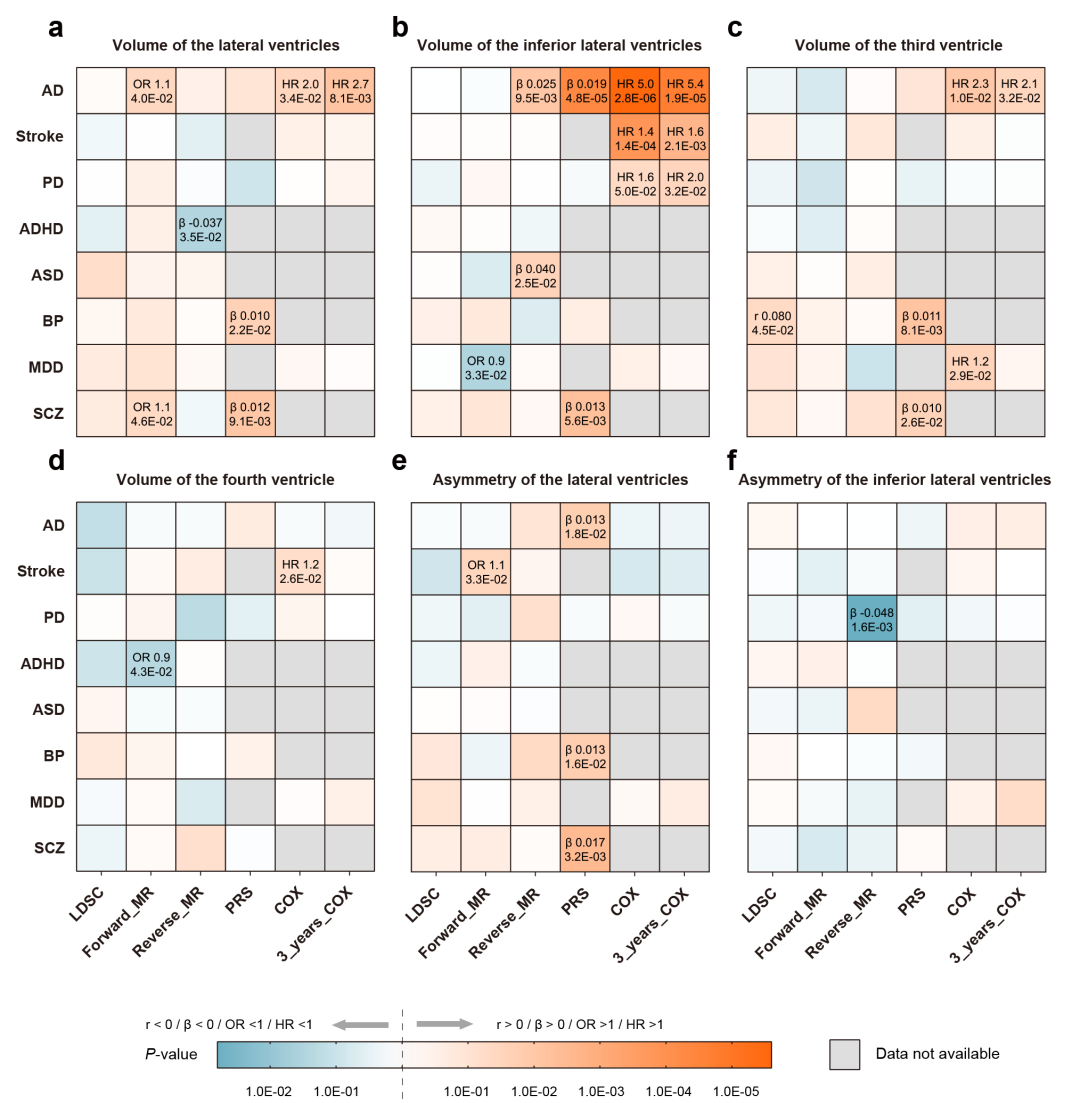
▲ 脑室形态和脑疾病存在遗传重叠
实验室主任冯建峰教授表示:“对于其他神经精神疾病,各分析方法并未得到一致的结论,因此结论证据水平相对较低。而对于阿尔茨海默病,多种分析结果共同支持侧脑室下角体积与阿尔茨海默病存在正向关联,且能经过独立队列的验证,因此该结论较为稳健。”
根据内表型假设,定义为内表型需满足以下标准:1)可遗传;2)与疾病相关;3)独立于个体的临床症状;4)在家庭中内表型和疾病共分离。基于以上标准,研究团队提出侧脑室下角体积是阿尔茨海默病的一个新内表型,可早期预测阿尔茨海默病的发病风险。由于侧脑室下角体积在临床环境中极易被评估,该研究成果具有较高的临床应用价值。
冯建峰教授补充:“大规模遗传影像的数据为我们探究脑结构的遗传基础奠定了数据基础,过去的研究都聚焦在大脑皮层及皮层下的脑结构,而对脑室缺乏相关研究,我们利用全生命周期的数据,首次系统地研究了脑室形态的遗传基础,这对我们理解脑室与脑疾病关系的内在机制,发现新脑疾病影像标志物,促进脑疾病的早期诊断、预测与进展评估具有重要意义。“
复旦大学类脑智能科学与技术研究院、计算神经科学与类脑智能教育部重点实验室程炜研究员、复旦大学附属华山医院神经内科郁金泰教授为该文的共同通讯作者,复旦大学附属华山医院神经内科博士生葛怡君、吴邦胜、张一为该文的共同第一作者。
该研究得到了英国生物样本库(UK Biobank)、国际”心脏与衰老研究基因组流行病学队列联盟”(CHARGE)、美国“青少年大脑认知发展”(ABCD)项目、欧洲“正常大脑功能和精神病理学中的强化相关行为”(IMAGEN)项目、美国”人脑连接组计划”(HCP)、美国”阿尔茨海默病神经影像学倡议”(ADNI)、复旦大学类脑智能科学与技术研究院、计算神经科学与类脑智能教育部重点实验室冯建峰教授、Gunter Schumann教授,复旦大学附属华山医院董强教授,青岛市市立医院谭兰教授等的大力支持和帮助。该研究得到了国家自然科学基金委、国家重点研发计划、上海市重大专项等的经费支持。
原文链接:
https://www.nature.com/articles/s41562-023-01722-6
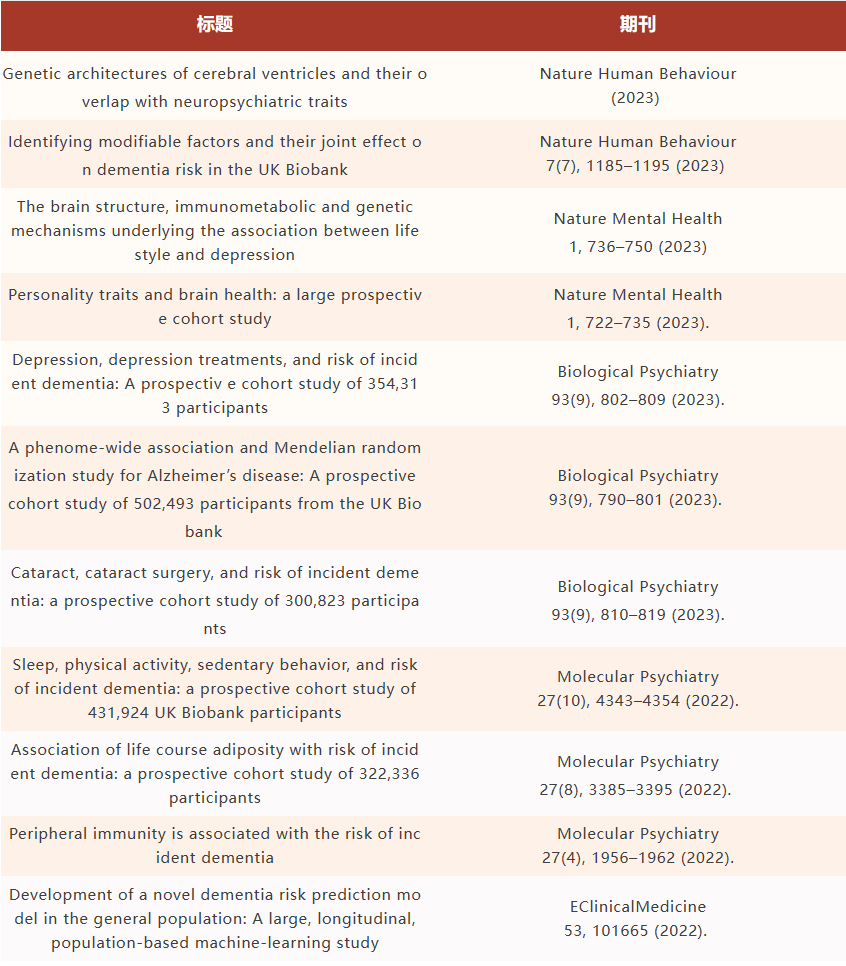
近年来,实验室冯建峰、程炜团队与复旦大学附属华山医院毛颖、郁金泰团队,基于双方医学大数据、智能算法与临床诊疗技术优势,建立理医工交叉联合攻关团队,在脑疾病早期智能预警、病理机制解析以及药物靶点研发等多个领域取得一系列突破。近三年,在Nature Human Behaviour,Nature Mental Health 等国际一流期刊合作发表论文30多篇,共同承担国家和上海市一系列重大项目,联合成立老年脑健康智能科学中心。未来,双方将进一步聚焦国家重大需求,发挥交叉研究综合力量,为推动重大脑疾病智能诊疗做出积极贡献。